
El pasado lunes, mediante una conferencia de prensa realizada en el Polo Científico Tecnológico, Daniel Filmus lanzó una nueva convocatoria a voluntaries para testear la vacuna argentina contra el COVID. El ministro de Ciencia, Tecnología e Innovación informó que la inyección ArVac-Cecilia Grierson se encuentra en fase 2/3, a la espera de ser evaluada en más personas.
Del anuncio también participó Juliana Cassataro, quien lidera el proyecto ArVac. Es investigadora de la Universidad Nacional de San Martín (UNSAM) y del CONICET.
Quienes deseen participar deben ser mayores de edad y contar con hasta tres dosis de vacunas contra COVID-19. También es requisito residir en la Ciudad Autónoma de Buenos Aires (CABA), La Plata, Mar del Plata, Córdoba capital, Mendoza capital y Salta capital.
En esta segunda etapa la convocatoria está abierta a 1.782 voluntaries, quienes participarán de la fase 2 y 3 de ensayos clínicos de la vacuna argentina diseñada para proteger contra las variantes presentes en la región. A diferencia de los requisitos para la primera etapa, les participantes podrán tener comorbilidades, excepto que tengan una deficiencia alta de la respuesta inmune.
Por su parte, las autoridades aspiran a que para fines de abril ya se cuente con la cantidad de voluntaries necesaries y, de este modo, concluir con la fase 2 y 3 en junio.
La responsabilidad de aprobarla o no estará a cargo de la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT).
💉 Ya podés participar del estudio clínico de la vacuna nacional #Arvac Cecilia Grierson, que protege contra las variantes de SARS-CoV-2 circulantes en la región. 🇦🇷Es un desarrollo de investigadores/as argentinos.
— Daniel Filmus (@FilmusDaniel) April 10, 2023
🖐️Ofrecete como voluntario/a entrando a: https://t.co/JdMRxH6DTf pic.twitter.com/6mBt8emzTE
ArVac-Cecilia Grierson: la primera vacuna nacional contra el COVID
La ArVac-Cecilia Grierson es una vacuna bivalente que cubre todas las variantes con mayor desarrollo hasta ahora en Argentina. En el caso de que surjan otras nuevas, en tres meses se estará en condiciones de producir la nueva vacuna sin necesidad de hacer todos los ensayos clínicos de nuevo. Esto se debe a que fue pensada para que sus refuerzos sean administrados de forma anual, según las variantes que estén en circulación.
Argentina es el único país de Sudamérica que está en condiciones de llevar adelante esta tarea. Además, es la primera vez que el país llega a la fase 2/3 de una vacuna para el COVID-19 con éxito.
La tecnología utilizada fue probada en otras partes del mundo y servirá para las distintas variantes, e incluso para otras vacunas. El objetivo es que sea una vacuna de alcance regional para que pueda ser exportada a otros países.
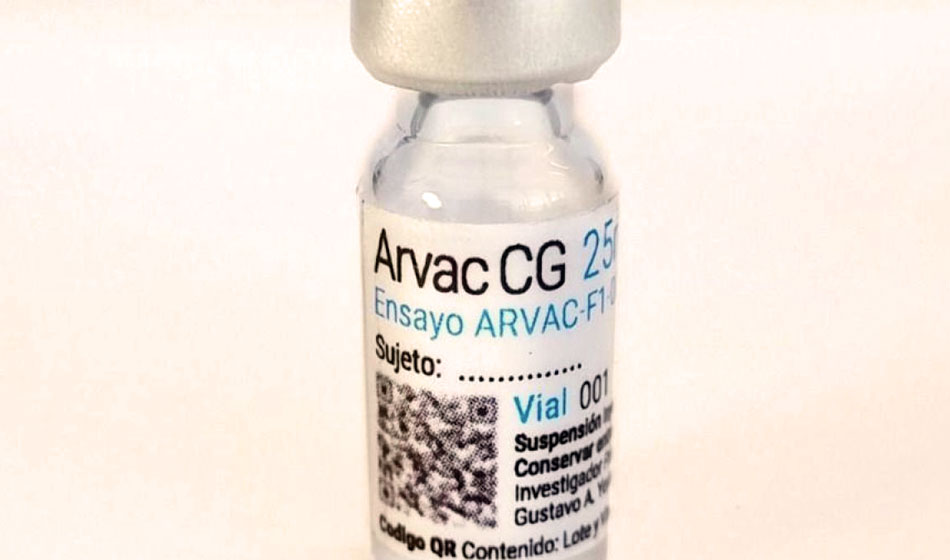
Según explicó Filmus, la vacuna ArVac-Cecilia Grierson continúa su avance luego de superar la fase 1, que es la etapa donde se comprobó su seguridad. Dado que los testeos en les primeres voluntaries funcionaron correctamente, crecen las expectativas de su eficacia.
“Concluyó la etapa uno de la fase 2/3 y para la segunda etapa ahora necesitamos 1.800 voluntarios más. En los 80 voluntarios de la fase 1 y los 260 de la primera parte de la fase 2/3 no hubo ningún efecto adverso grave”, detalló Cassataro.
Por su parte, el director comercial del Laboratorio Cassará, Jorge Cassará, informó que “con los datos que tenemos de la fase 1 ya sabemos que aumenta significativamente, hasta 30 veces, los anticuerpos neutralizantes contra las distintas variantes”. “Ahora agregamos una versión, que está en la fase tres, que es una bivalente con la variante Ómicron», explicó.
Los pasos para aprobar una vacuna
Existen diferentes pruebas que deben superar las vacunas para ser aprobadas. Entre ellas se destacan las que aseguran su seguridad para que no produzcan efectos adversos indeseables. También aquellas que determinan su eficacia para producir una correcta respuesta inmune.
Durante la fase 1, en la que se evaluó su seguridad, se probó la vacuna en 80 personas. Una vez superada, comenzó la primera etapa de la fase 2/3. En enero de este año, se administró la vacuna a 232 personas. Fue aplicada sólo en los centros CEMIC y Clinical Pharma, de la Ciudad Autónoma de Buenos Aires. En esta segunda etapa se busca administrarla en 10 centros distribuidos en CABA, Buenos Aires, Mendoza, Salta y Córdoba.

La vacuna es proteica, con una tecnología muy segura, ya que es la misma tecnología con la que se vacunan niñes y recién nacides desde hace 30 años contra la Hepatitis B, y más recientemente en adolescentes.
Para obtener más información y postularse, ingresá a: https://arvac.com.ar/.

